GAZ BASINCI
Gazların basıncını iki başlık altında inceleyeceğiz.
Açık Hava Basıncı
Açık hava basıncını keşfeden fizikçi Evangelista Torricelli olmuştur.
Toricelli atmosferi oluşturan gazların Dünya'ya uyguladığı basıncı kurduğu deney düzeneği ile ispatladı.
Deniz seviyesinde 0°C de ağzı açık civa dolu bir kap içerisine bir cam boru daldırdı.
Bu düzenekten beklediği sonuç, havadaki moleküller civaya basınç uygularsa cam boruda civa yükselmeliydi. Deney beklediği gibi sonuçlandı, civa da 76 cm yukselme gözlemlendi.
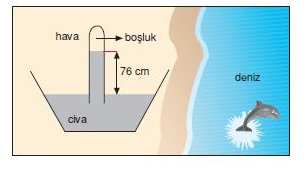
Bu deneyden çıkarılan sonuç;
Açık hava basıncı
Borudaki civanın yükselme miktarı
Kapalı Kaplarda Gaz Basıncı
Kapalı bir kaba gaz konulduğunda gaz molekülleri kabin çeperlerine basınç uygular.
Gaz moleküllerinin titreşerek kabın iç çeperlerine çarpması sonucu oluşur.
Kapalı kap içerisindeki gaz moleküllerinin basıncı;
P.V= n. R. T
ile ifade edilir. Bu denkleme ideal gaz denklemi denir.
P: gaz basıncı
V: hacim
n: molekül sayısı
R: gaz sabiti
T:sıcaklık
Bu denklem göz önünde bulundurularak;
(T ile doğru orantılı)
(n ile doğru orantılı)
(V ile ters orantılı)
Manometreler
Kapalı kaplarda gaz basıncı manometre ile ölçülür.
Manometrelerin çalışma prensibi U borusu mantığına dayanır.
Manometrenin iki kolundaki basınçlar birbirine eşittir. Gazın basıncı bu eşitliğe dayanılarak bulunur.
Kapalı Uçlu Manometre
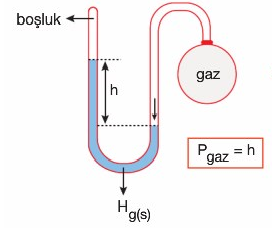
Açık Uçlu Manometreler
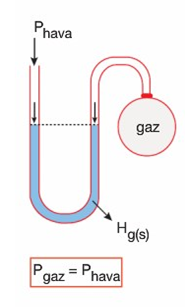
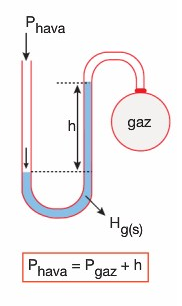
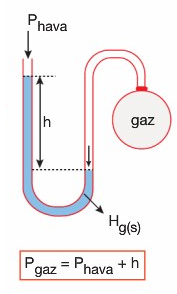
Basınç Ölçmek İçin Kullanılan Aletler
ÖRNEK:
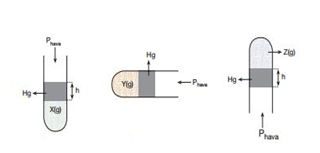
Yukarıda verilen cam tüplerdeki X, Y, Z gazlarının basıncını büyükten küçüğe doğru sıralayınız.
ÇÖZÜM:
PX =Phava+PHg
Py =Phava
Pz =Phava-PHg
PX >PY >PZ
ÖRNEK:
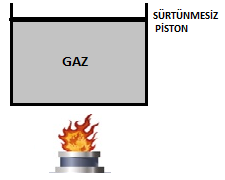
Yukarıdaki şekildeki içi gaz dolu kap ısıtıldığında gazın basıncı hakkında ne söylenebilir?
ÇÖZÜM:
Gaz ısıtılınca sıcaklığı artar. Buna bağlı olarak genleşeceğinden hacmi artar.
P.V= n. R. T
P (gaz basıncı) bu durumda sabit kalır.