
Gazların Sıkışma ve Genleşme Özelliği Gazların sıkıştırılabilmeleri fiziksel bir özelliktir. Sıkıştırma ile gazlar birbirlerine daha çok yaklaşırlar ve aralarındaki uzaklık azalır. Böylece sıkıştırma maddenin fiziksel halinin değişmesine sebep olabilir. Gazlar sıcaklıkları azaltılıp basınçları arttırıldığında sıvılaşma özelliği kazanmaktadır. Sıvılaştırılmış gazlar ise hayatımızın çeşitli alanlarında kullanılmaktadır.
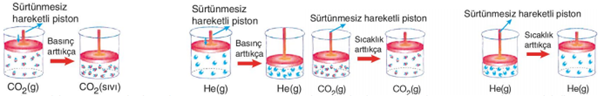
Kaplar içindeki CO2 ve He gazları basınçla sürtünmesiz piston sayesinde sıkıştırılmaktadır. Basınç arttıkça CO2 ve He gazlarının molekülleri arasındaki uzaklık azalır. Bunun sonucunda CO2 gazı, moleküller arasındaki çekim kuvvetinin artmasıyla sıvılaşır. Ama uygulanan basınç He' un sıvılaşmasını sağlayamaz. Bu durumda CO2 gazını gerçek gaz, He gazını ise ideale yakın gaz olarak nitelendirebiliriz. Moleküller arası etkileşimi olan ve moleküllerin birbirinden etkilendiği gazlara gerçek gazlar denir. Molekülleri arasındaki etkileşimlerin sonucunda gerçek gazlar basınçla sıvılaşabilir. Gerçek gazlarda moleküllerin hacmi ihmal edilemez. Molekülleri arasında etkileşim (çekim kuvveti) olmayan, moleküllerinin davranışları birbirinden etkilenmeyen ve moleküllerinin hacmi çok küçük olduğundan toplam hacim yanında ihmal edilebilen gazlara ideal gaz denir. Doğada bulunan gazların hiçbiri ideal gaz değildir. Ancak gerçek gazlar yüksek sıcaklık ve düşük basınçta idealliğe yaklaşır. Yukarıdaki şekillerde de görüldüğü gibi CO2 ve He gazlarının sıcaklığı arttıkça, moleküllerin ortalama kinetik enerjileri artar ve daha hızlı hareket etmeye başlarlar. Kabın çeperlerine çarpma sayıları da artar. Çarpma sonucunda oluşan itme kuvvetlerinin etkisiyle sürtünmesiz piston yukarı doğru hareket eder. Kabın hacmi de artmış olur. Sıcaklığın artmasıyla gaz moleküllerinin hareketliliğinden kaynaklanan hacim değişimine ısıl genleşme adı verilir. CO2 gazındaki ısıl genleşme, He gazındaki ısıl genleşmeden daha az olmuştur. Bunun sebebi He gazının ideale daha yakın olmasıdır.
İdeal gazlarda;

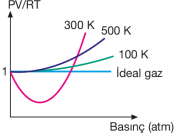
İdeal Gaz Durumundan Sapmalar Genellikle gerçek gazlar her koşulda PV = nRT formülüne tam olarak uyamazlar. 1 mol ideal gaz için PV = nRT eşitliği uygulandığında PV/RT = 1 olur. Yandaki grafik değişik sıcaklıklarda CH4 gazının PV/RT oranının basınçla değişimini göstermektedir. İdeal gazlar için PV/RT oranı her sıcaklık ve basınçta 1'dir.

FAZ DİYAGRAMI Birbiriyle temasta olan birkaç kısımdan oluşan bir sistemin her bir homojen olan kısmına faz denir. Faz diyagramı ile arı bir maddenin belirli dış basınç ve sıcaklıktaki fiziksel hali belirlenir. Aşağıda saf su ve CO2'nin faz diyagramları verilmiştir.
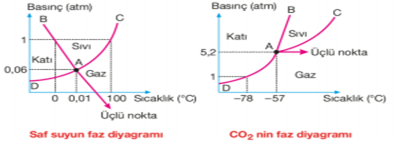
AB, AC ve AD eğrileri düzlemi üç bölgeye ayırır. Maddenin sıcaklık ve basıncının kesiştiği nokta hangi bölgeye düşerse, madde o fiziksel haldedir.
AB eğrisi : Katı - sıvı denge durumunu belirler. Bu eğri üzerindeki noktalar maddenin çeşitli basınçlardaki donma noktalarını (veya erime noktalarını) gösterir.
AC eğrisi : Sıvı - gaz denge durumunu belirler. Bu eğri üzerindeki noktalar maddenin çeşitli basınçlardaki kaynama noktalarını (veya yoğunlaşma noktalarını) gösterir.
AD eğrisi : Katı - gaz denge durumunu belirler. Bu eğri üzerindeki noktalar maddenin çeşitli basınçlardaki süblimleşme noktalarını (veya kırağılaşma noktalarını) gösterir.
A noktası : Üçlü nokta denir. Maddelerin katı, sıvı ve gaz hallerinin tümünün aynı ortamda bir arada bulunabildiği sıcaklık ve basınç değerine üçlü nokta denir. Suyun faz diyagramında katı - sıvı eğrisi biraz sola yatıktır. Eğri incelendiğinde dış basınç arttıkça suyun donma noktasının düştüğü görülür. CO2'nin faz diyagramında katı - sıvı eğrisi biraz sağa yatıktır. Eğri incelendiğinde dış basınç arttıkça donma noktasının yükseldiği görülür. Tüm maddelerin faz diyagramında katı - sıvı eğrisi, sıcaklık eksenine dike yakındır. Bu nedenle basıncın donma noktasına etkisi çok azdır.
JOULE THOMSON OLAYI Herhangi bir maddeyi soğutmanın yollarından birisi kendisinden daha soğuk başka bir maddenin içine koymaktır. Buz, sıvı hava, kuru buz (katı CO2), aseton - alkol veya aseton - eter karışımı bu amaçla kullanılan soğutucu maddelerdendir. Bu konu hakkında ilk defa çalışan bilim insanları James Prescott Joule ve William Thomson'dur.
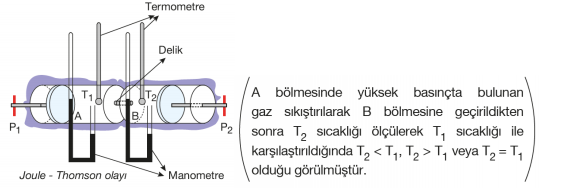
Joule ve Thomson yaptıkları deneyin sonucunda hızla genleştirilen gazların farklı davrandıklarını, bazı gazların sıcaklığında değişiklik olmadığı, bazı gazların ısındığı, bazı gazların ise soğuduğunu gözlemlemişlerdir. Gazlar genleştirildiklerinde, moleküller birbirinden uzaklaşırlar ve bundan dolayı gazların hacimlerinin artmasıyla moleküller birbirinden ayrılarak ortalama hızları düşer. Genişleyen gazın molekülleri arasındaki çekim kuvvetlerinin yenilmesi için gereken enerji dış ortamdan alınamayacağından dolayı gaz moleküllerinin öz ısıları kullanılarak karşılanır. Bu şekilde genleştirilen gazlar hızla soğurlar. Soğuyan gaz bulunduğu ortamı da soğutur. Bu gözleme Joule - Thomson olayı adı verilir. Joule - Thomson olayının uygulamalarına buzdolabı, klima ve derin dondurucuların soğutulması, bisiklet sibobunda soğuma, pompada sıkışan gazın ısınması gibi örnekler verilebilir. Joule - Thomson olayı sonucunda genleşme sırasındaki sıcaklık değişimi ne kadar küçük ise gaz ideale o kadar yakındır.

Gaz, Buhar ve Kritik Sıcaklık Bulunduğu sıcaklıkta, hiçbir basınç altında sıvılaştırılamayan sıkıştırılabilir akışkanlara gaz denir. Gazların sıcaklığı arttıkça, sıvılaştırılmaları zorlaşır ve basınç uygulanması gerekir. Ancak gazlar için bazı sıcaklıklar vardır ki, bu sıcaklığın üstünde ne kadar basınç uygulanırsa uygulansın sıvılaştırılamazlar. Her gaz için ayrı olan bu sıcaklığa kritik sıcaklık adı verilir. Kritik sıcaklık, bir gazın basınç uygulanarak sıvılaştırılabileceği en yüksek sıcaklıktır ve TK ile gösterilir. Gazlar gibi davrandıkları halde, bulundukları sıcaklıkta basınçla sıvılaştırılabilen akışkanlara buhar adı verilir. Buhar ile gaz arasında bir dönüşüm yoktur. Buhar özelliğinin ortadan kalkarak gaz özelliğinin başladığı sıcaklık, kritik sıcaklıktır. Buharlaşırken ortamdan ısı alarak bulunduğu ortamın soğumasına sebep olan maddelere soğutucu akışkanlar denir. Soğutucu akışkan olarak kullanılacak maddenin basınçla sıvılaştırılabilmesi ve üzerindeki basınç kaldırıldığında buhar hale geçmesi gerekmektedir.
Soğutucu akışkanların sahip olması gereken bazı özellikler aşağıda verilmiştir.
En çok kullanılan soğutma akışkanları şunlardır: Freon 22, Freon 134a, Freon 407c, Freon 410A (Ozona zararsızdır. ) 407c'nin muadili olup daha verimli olduğundan 407c nin yerini tamamen almıştır.