Elektrolizin Nicel İncelenmesi (Faraday Yasası)
Michael Faraday, 1833 yılında elektroliz ile ilgili iki tane yasa belirlemiştir.
Faraday’ın I. elektroliz kanununa göre; Elektrolizde anot ve katotta açığa çıkan madde miktarları devreden geçen elektrik yükü miktarı ile doğru orantılıdır.
Faraday’ın II. elektroliz kanununa göre: "Aynı miktarda elektrik yükü geçen farklı elektrolitlerin elektrolizi sırasında her bir hücre elektrotlarında, elde edilen madde miktarları bu maddelerin eşdeğer kütleleriyle doğru orantılıdır.
Devreden 1 mol elektronun yükü geçince 1 eşdeğer gram madde açığa çıkar. Bir maddenin atom kütlesinin değerliğine oranı eşdeğer kütleyi verir. 1 mol elektronun yükü 1 faradaylık yüktür ve 96500 coulomb elektrik yüküdür.
1 mol elektron = 1F=96500 coulomb Q=l.t
Eşitliği kullanılarak da devreden geçen toplam elektrik yük miktarı bulunabilir.
Q: yük miktarı, birimi coulomb
I: akım şiddeti, birimi amper
t: zaman, birimi saniye
Endüstriyel Elektroliz Uygulamaları
Elektroliz endüstride birçok alanda kullanılır. Bunlardan öne çıkanlar, korozyon, kaplamacılık, metallerin saflaştırılması ve elementlerin eldesi olarak ifade edilebilir. Korozyon Elektrokimyasal işlemler sonucu metallerin aşınmasına korozyon denir.
Demirin paslanması, gümüşün kararması korozyona örnektir. Demirin paslanmasında hem yükseltgenme hem de indirgenmenin olması için ortamda oksijen ve suyun bulunması gerekir.
Demirin bir kısmı anot olarak davranır ve bu bölümde Fe(k) à Fe+2 (suda) + 2e tepkimesi gerçekleşir. Metalin diğer bir kısmında ise havadaki oksijen indirgenir, bu bölümde katot olarak ifade edilir.
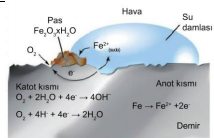
Oluşan Fe+2 iyonu asidik ortamda tekrar oksijen ile tepkime vererek Fe2O3 (pas) oluşturur. Korozyonun önlenebilmesi için, metalin nemden ve oksijenden uzak tutulması gerekir. Bunun için genellikle metaller boyanır. Boru hattı yeraltı su ve yakıt depoları gibi sistemlerde korozyonun önlenmesi için daha aktif bir elektrot kurban elektrot olarak kullanılır. Bu sayede demir yerine sisteme bağlanan Mg gibi kurban elektrotlar aşınır.
Kaplamacılık: Metalleri korozyondan korumak ve iyi bir görünüme sahip olmalarını sağlamak için metallerin yüzeyi korozyona dayanıklı başka bir metal ile kaplanabilir. Kaplama yapılacak metal katot olarak, kaplama yapılacak metalin çözeltisi içerisine daldırılır. Anot olarak genelde çözeltideki kaplama için kullanılan iyonun metali kullanılır.
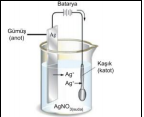
Şekilde bir kaşık nikel ile kaplanmaktadır. Katotta metal +2 kaşık, anotta nikel metal vardır ve Ni çözeltisi içerisine anot ve katot yerleştirilmiştir. Kapı kolları, musluk ve bataryalar, birçok araba aksesuarı korozyona karşı nikel, krom gibi metallerle kaplanır. Metalin ne kadar kaplanacağı devreden geçen akımın ve sürenin ayarlanması ile sağlanır. Ayrıca kaplamanın homojen olması ve yüzeyde yanık oluşmaması için çözelti veya kaplanacak parça işlem boyunca hareket ettirilir.
Metallerin Saflaştırılması: Bakır gibi metaller elde edildiklerinde genellikle çinko, demir gibi bazı metalleri barındırırlar. Safsızlığa neden olan bu metaller elektroliz ile ayrıştırılır. Şekildeki düzenekte bakırın saflık derecesi %99,5 üzerine kadar çıkarılır. Burada anotta saf olmayan külçe ayrışırken katotta saf bakır toplanır.
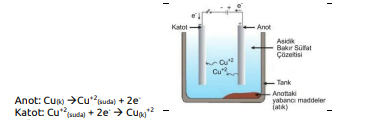
Safsızlığa neden olan Fe, Zn, Au, Ag gibi maddeler Cu iyonuna göre daha zor indirgendiğinden çözelti içerisinde iyon olarak veya elektrot üzerinde metal olarak kalırlar.
Metal Eldesi : Alüminyum gibi bazı elementler cevherlerinden elde edilirken öncelikle çözeltide iyon halinde elde edilirler. Bu iyonların katı metale dönüşmesi için uygun koşullarda indirgenmesi gerekir. Bunun için de elektroliz işlemi uygulanır.
Örneğin alüminyum eldesi sırasında çözelti elektroliz edilirse
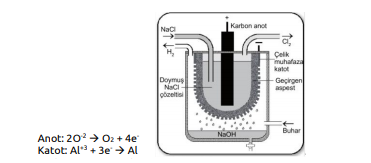
tepkimesi sonucu alüminyum metali ve oksijen gazı elde edilir. Elde edilen alüminyum miktarı devreden geçen akımla doğru orantılıdır. Metal eldesi, saflaştırılması, sudan hidrojen eldesi yanı sıra önemli bir elektroliz uygulaması da endüstriyel NaOH üretimidir. NaOH üretimi gerçekte sulu NaCI çözeltisinin özel bir elektroliz kabında elektrolizinden başka bir şey değildir. Bu sistemde anotta Cl2 gazı ve katotta H2 gazı açığa çıkarken NaOH çözeltisi başka bir kaba alınarak buharlaştırılır. Böylece katı NaOH elde edilir.
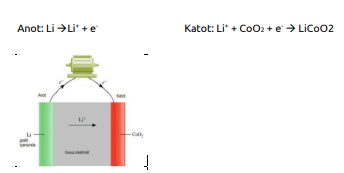
Lityum İyon Pilleri (Li-ION): Lityum iyon pilin temel ilkesi şudur: Dolma ve boşalma işlemi, temelde yalnızca lityum iyonların iki elektrot arasındaki transferi aracılığıyla gerçekleşir. Pil dolarken lityum iyonlar karbondan yapılmış grafit bir katmana transfer edilir. Boşalma sırasında iyonlar geri gider. İyonların geçişi elektron akışını kontrol eden elektromanyetik bir güç yaratır. Lityum iyon pillerde, artı uç lityum metal oksitten ve eksi uç karbondan yapılmıştır. Bu piller aynı zamanda bir elektronik devre içerir. Böylece pillerin ne kadarının dolu olduğu ne kadarının boş olduğu kaydı sürekli tutulduğundan tamamen boşalmadan da bu piller tekrar şarj edilebilir. Ancak pilin kullanım ömrü üretim tarihinden itibaren başlar. Li-ion piller hafiftir. Cep telefonları, tabletler ve bilgisayarların çoğunluğu artık li-ion pil kullanılmaktadır.
Lityum iyon pillerinin bu özelliklerinden başka kullanım avantajları şunlardır:
• Tekrar şarj edilerek defalarca kullanılabilir.
• Karbondioksit salınımı çok az olduğundan ve toksik madde içermediğinden çevreye verdiği zarar azdır.
• Kütlesinin küçük, ürettiği enerji miktarının fazla olmasından dolayı dizüstü bilgisayar, tablet ve cep telefonu gibi elektronik eşyalarda yaygın olarak kullanılır.
Korozyon : Bir maddenin çeşitli etkiler sonucunda kimyasal olarak aşınmasına korozyon (paslanma, çürüme) denir. Her ne kadar seramik, ahşap, plastik vb. maddeler çevre şartlarından dolayı bozulma gösterse de korozyon terimi genellikle metaller için kullanılır. Metaller özellikle nemli ortamlarda havadaki oksijenle yükseltgenip metal oksitleri oluşturur ve bu olayın sonucunda korozyona uğrar .
Korozyona Karşı Alınabilecek Önlemler
• Metalleri boyamak
• Korozyona dayanıklı malzemeler kullanmak
• Metali başka bir metalle kaplamak • Katodik koruma sistemleri kullanmak
Kurban Elektrot
Bir metali korozyondan korumak için metale, aktifliği bu metalden daha fazla olan bir metal bağlanır. Bağlanan bu metale kurban elektrot denir. Katodik korumada kurban elektrot anot işlevi görür. Örneğin bir demir parçası daha aktif olan magnezyum metali ile kaplanırsa magnezyum metali kurban elektrot olur. Metal borular, deniz araçları, sıvı tankları, LPG tankları ve su sistemleri kurban elektrodun kullanım alanlarından bazılarıdır.
Katodik korumada magnezyum, alüminyum, çinko gibi aktif metaller, korozyondan korunacak cisme doğrudan ya da bir tel yardımıyla bağlanır. Aktif metal yükseltgenirken demir ya da çelik yüzey açığa çıkan elektronları alır ve katot görevi görür. Bu korumada aktif metal anot yani kurban elektrottur. Gemiler, depolama tankları, boru hatları ve su tesisatları gibi suyla ya da nemli toprakla doğrudan temas hâlindeki demir ve çelikten yapılmış cisimleri korumak için genellikle alüminyum ve magnezyum metalleri, kurban elektrot olarak kullanılır.